技术平台
基于光亲和磁珠技术
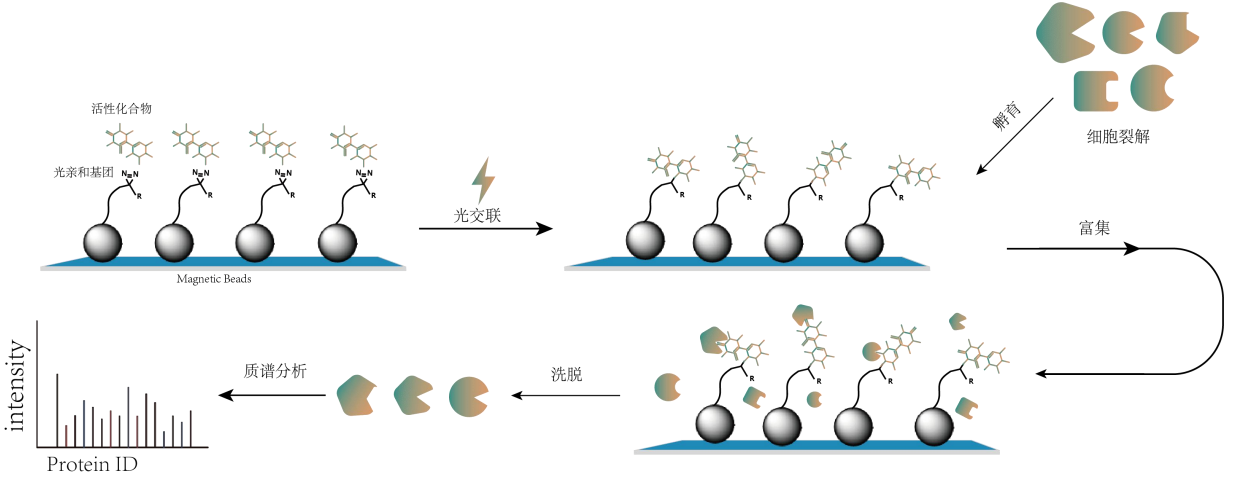
化学蛋白质组学技术在药物靶点发现中迅速发展,尤其是基于化学探针的平台。该技术已成功应用于化学小分子药物、天然产物、已批准老药及内源性代谢物。然而,开发化学探针面临着诸如合成复杂、产率低、成本高及药物分子SAR(Structure-Activity Relationship) 不明,这些因素极大地限制了靶点发现和机制解析。
基于光亲和磁珠的药物靶点发现平台通过光照将活性药物分子固定在功能性磁珠上,避免了化学探针的设计和合成,同时减少药物结构变化,保证药物分子与靶点蛋白质之间的特异性结合。固载有活性药物分子的磁珠与蛋白质组孵育后,可富集和分离药物靶点蛋白质,用于免疫印记和质谱分析。
平台特点
√无需合成探针,节省实验时间和成本
√适用于难以进行结构改造的药物分子
案例展示
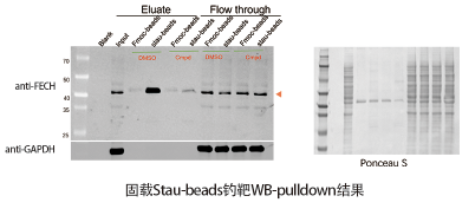
为验证staurosporine(Stau)的靶点,我们将其固定于光亲和修饰的功能性磁珠表面(以下简称Stau-beads)。随后将Stau-beads与全蛋白质组孵育,Fmoc-beads作为对照组。
所得WB结果如下图所示,Stau-beads能有效富集目的蛋白FECH(已知阳性靶点)。
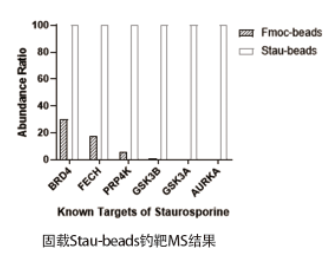
接下来,我们将Fmoc-beads和stau-beads富集分离的蛋白质进行酶切,质谱检测,定量比较实验组与对照组中蛋白质的强度差异。结果表明,所有已知的阳性靶点蛋白质均在Stau-beads组中被显著性富集,证实了方法的有效性。
相关文献
※通过光亲和磁珠固定化甲基格尔费林(M-GFN),鉴定乙二醛酶 I(GLO1)为直接靶点,其抑制 GLO1 活性导致甲基乙二醛累积,阻断 NFATc1 信号通路,从而特异性抑制破骨细胞生成,为骨质疏松治疗提供新策略。The identification of an osteoclastogenesis inhibitor through the inhibition of glyoxalase I.Proc Natl Acad Sci U S A. 2008 ;105(33):11691-6.(IF:9.1)
※光亲和磁珠技术结合质谱分析鉴定出天然化合物 Corylin 特异性靶向 HSP90β中间结构域,通过 Akt-GSK3β-FBW7,促进 SREBPs 泛素化降解,从而显著改善肥胖、脂肪肝及动脉粥样硬化等脂代谢紊乱。Inhibition of HSP90β Improves Lipid Disorders by Promoting Mature SREBPs Degradation via the Ubiquitin-proteasome System. Theranostics. 2019;9(20):5769–5783.(IF:13.2)