基于蛋白质热稳定性变化技术
利用小分子配体(探针或药物)与靶蛋白结合后,通常会改变靶蛋白自身热稳定性的特点;在此基础上,通过细胞热迁移实验(CETSA)结合质谱技术,即可系统性检测全蛋白质组中,因配体存在而发生热稳定性变化的蛋白(这类蛋白即潜在的配体作用靶蛋白)。
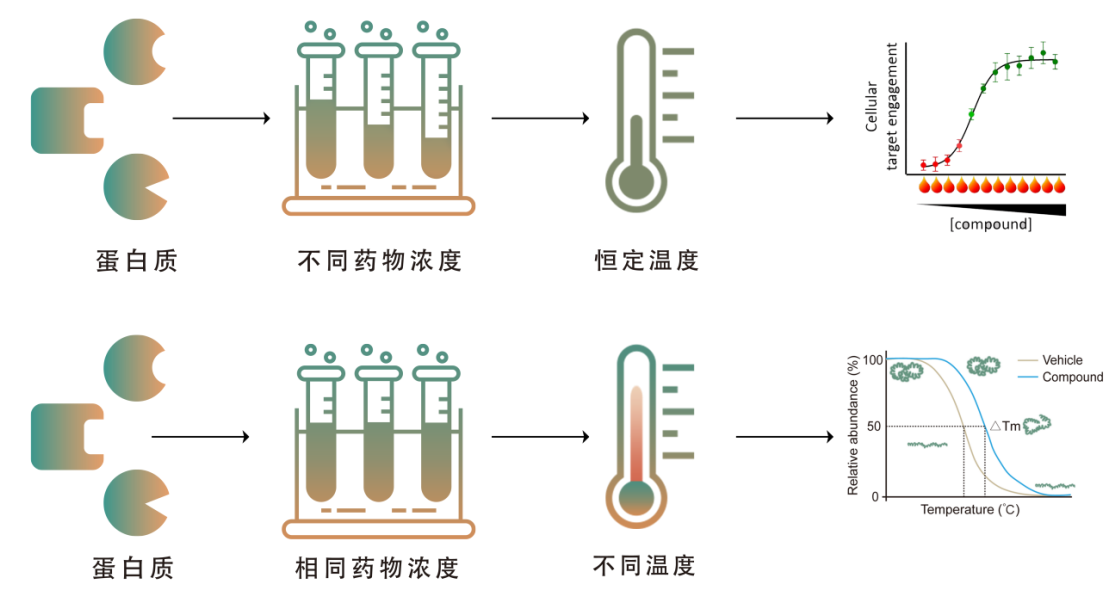
技术平台
利用小分子配体(探针或药物)与靶蛋白结合后,通常会改变靶蛋白自身热稳定性的特点;在此基础上,通过细胞热迁移实验(CETSA)结合质谱技术,即可系统性检测全蛋白质组中,因配体存在而发生热稳定性变化的蛋白(这类蛋白即潜在的配体作用靶蛋白)。

√可在无修饰、接近生理环境的全细胞裂解物或活细胞中进行。
√无需预先设计特定探针(可直接测试药物分子)。
√能无偏性地发现配体的直接和间接作用靶点以及脱靶效应。
项目需求:以热稳定实验,在细胞裂解液中,验证目标小分子与靶蛋白是否直接结合。
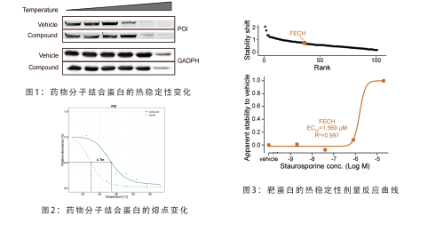
解决方案:分别利用免疫印迹(图1)和温度梯度的蛋白质热稳定性分析TPP-TR(图2)、小分子浓度梯度的蛋白质热稳定性分析TPP-CCR(图3),对目标蛋白的热稳定性进行分析。
数据展示:
※采用METAL-TPP技术实现全蛋白质组水平金属结合蛋白(MBPs)的无标记筛选,发现锌离子抑制GFPT2酶活并调控己糖胺通路。本研究为北京大学王初教授(科络思生物首席科学家、联合创始人)课题组工作。Discovery of metal-binding proteins by thermal proteome profiling .Nat Chem Biol, 2024, 20, 770–778.(IF: 13.5)
※热蛋白质组分析(TPP)揭示衣康酸(itaconate)通过共价修饰KEAP1(Cys151)激活NRF2抗氧化通路,并靶向代谢酶ACLY、SDH重塑巨噬细胞免疫代谢网络,实现抗炎与氧化应激防御双重调控。本研究为北京大学王初教授(科络思生物首席科学家、联合创始人)课题组工作。Thermal proteome profiling of itaconate interactome in macrophages. Chem Sci. 2025 ;16(30):13838-13846.(IF:8.9)